ANSM - Mis à jour le : 24/08/2007
SUCCESSIA 1 mg/0,025 mg, comprimé pelliculé
Veuillez lire attentivement l'intégralité de cette notice avant de prendre ce médicament.
Dans cette notice :
1. QU'EST-CE QUE SUCCESSIA 1 mg/0,025 mg, comprimé pelliculé ET DANS QUELS CAS EST-IL UTILISE ?
2. QUELLES SONT LES INFORMATIONS A CONNAITRE AVANT DE PRENDRE SUCCESSIA 1 mg/0,025 mg, comprimé pelliculé ?
3. COMMENT PRENDRE SUCCESSIA 1 mg/0,025 mg, comprimé pelliculé ?
4. QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ?
5. COMMENT CONSERVER SUCCESSIA 1 mg/0,025 mg, comprimé pelliculé ?
6. INFORMATIONS SUPPLEMENTAIRES
1. QU'EST-CE QUE SUCCESSIA 1 mg/0,025 mg, comprimé pelliculé ET DANS QUELS CAS EST-IL UTILISE ?
ESTROGENES ET PROGESTATIFS, POUR ADMINISTRATION SEQUENTIELLE.
Ce médicament est une association d'un estrogène et d'un progestatif pour administration continue séquentielle.
Ce traitement est préconisé dans le traitement des troubles dus à un déficit en estrogènes lié à la ménopause.
SUCCESSIA est indiqué dans la prévention de l'ostéoporose post-ménopausique chez la femme ayant un risque accru de fracture ostéoporotique et présentant une intolérance ou une contre-indication aux autres traitements indiqués dans la prévention de l'ostéoporose.
Le choix de ce traitement doit être discuté avec votre médecin.
L'expérience de ce traitement chez la femme âgée de plus de 65 ans est limitée.
Liste des informations nécessaires avant la prise du médicament
Sans objet.
Ne prenez jamais SUCCESSIA 1 mg/0,025 mg, comprimé pelliculé dans les cas suivants:
·hyperplasie de l'endomètre (développement exagéré de la muqueuse utérine);
·porphyrie (maladie héréditaire).
Précautions d'emploi ; mises en garde spéciales
Faites attention avec SUCCESSIA 1 mg/0,025mg, comprimé pelliculé:
Un examen médical est nécessaire avant et périodiquement en cours de traitement. A intervalles réguliers (au moins une fois par an), votre médecin sera amené à discuter avec vous des bénéfices et des risques associés avec un traitement hormonal substitutif afin d'évaluer si vous devez poursuivre ou arrêter votre traitement.
Un examen clinique régulier des seins sera effectué par votre médecin, en particulier en cas d'antécédents de cancer du sein dans votre famille ou si vous présentez des kystes ou des nodules des seins. Votre médecin pourra également être amené à vous prescrire une mammographie. Prévenez votre médecin si vous constatez une modification de vos seins pendant le traitement.
Les femmes qui utilisent un traitement hormonal substitutif ont un risque augmenté de développer une maladie thrombo-embolique, un cancer du sein ou de l'utérus, un accident cardiovasculaire ou un accident vasculaire cérébral.
Signalez à votre médecin toute maladie survenant en cours de traitement. Dans les situations suivantes, le traitement de la ménopause n'est pas contre-indiqué mais nécessite une surveillance particulière: hypertension artérielle, diabète, endométriose (affection caractérisée par la présence de muqueuse utérine en dehors de l'utérus), fibrome utérin, troubles hépatiques ou biliaires, épilepsie, migraine ou maux de tête sévères, insuffisance rénale ou cardiaque, asthme, lupus (maladie sévère atteignant notamment la peau), otospongiose (affection de l'oreille entraînant une baisse de l'audition).
Prévenez immédiatement votre médecin en cas d'apparition des signes suivants:
Prévenez votre médecin si vous devez rester alitée ou si vous devez subir une intervention chirurgicale.
Si les symptômes de déficit en estrogènes liés à la ménopause persistent malgré le traitement, parlez-en à votre médecin.
Si des saignements abondants surviennent, consultez votre médecin.
En raison de la présence de lactose, ce médicament ne doit pas être utilisé en cas de galactosémie, de syndrome de malabsorption du glucose et du galactose ou de déficit en lactase (maladies métaboliques rares).
Interactions avec d'autres médicaments
Prise ou utilisation d'autres médicaments:
Veuillez indiquer à votre médecin ou à votre pharmacien si vous prenez ou avez pris récemment un autre médicament notamment des anti-convulsivants, des anti-tuberculeux ou des traitements du SIDA tels que: la carbamazépine, l'oxcarbazépine, le phénobarbital, la phénytoïne, la rifabutine, la rifampicine, le ritonavir, le nelfinavir, la névirapine, l'éfavirenz, ou des préparations à base de plantes contenant du millepertuis (Hypericum perforatum), même s'il s'agit d'un médicament obtenu sans ordonnance.
Interactions avec les aliments et les boissons
Sans objet.
Interactions avec les produits de phytothérapie ou thérapies alternatives
Sans objet.
Utilisation pendant la grossesse et l'allaitement
Grossesse et allaitement
Ce médicament n'a pas d'indication pendant la grossesse ou l'allaitement.
Si vous découvrez que vous êtes enceinte alors que vous prenez ce médicament, interrompez le traitement et parlez-en à votre médecin.
La découverte d'une grossesse exposée par mégarde à ce médicament ne justifie pas l'interruption de grossesse.
Demandez conseil à votre médecin ou à votre pharmacien avant de prendre tout médicament.
Sans objet.
Effets sur l'aptitude à conduire des véhicules ou à utiliser des machines
Sans objet.
Liste des excipients à effet notoire
Liste des excipients à effet notoire: lactose.
3. COMMENT PRENDRE SUCCESSIA 1 mg/0,025 mg, comprimé pelliculé ?
Instructions pour un bon usage
Sans objet.
Posologie, Mode et/ou voie(s) d'administration, Fréquence d'administration et Durée du traitement
Mode et voie d'administration
Voie orale.
Prendre 1 comprimé beige par jour pendant 16 jours, puis 1 comprimé bleu par jour pendant les 12 jours suivants.
Avalez le comprimé avec de l'eau pendant ou entre les repas, de préférence à la même heure.
Il s'agit d'un traitement continu, c'est-à-dire que dès que vous avez terminé une plaquette, commencez la plaquette suivante dès le lendemain (débutez par un comprimé beige).
S'il s'agit de votre premier traitement hormonal substitutif de la ménopause ou si vous preniez un traitement hormonal substitutif combiné continu, vous pouvez débuter votre traitement n'importe quel jour de la semaine à votre convenance.
Par contre, si vous preniez déjà un traitement hormonal séquentiel, le traitement par SUCCESSIA 1mg/0,025 mg, comprimé enrobé devra débuter le jour suivant la fin du traitement séquentiel, sauf avis contraire de votre médecin.
Les règles surviennent généralement pendant les premiers jours d'utilisation d'une nouvelle plaquette et durent en moyenne 4 à 5 jours. Des saignements irréguliers peuvent survenir au cours des premiers mois de traitement. Au-delà des premiers mois de traitement, si des saignements abondants et/ou irréguliers surviennent, consultez votre médecin.
|
Comment démarrer votre plaquette: |
Exemple:
Si vous commencez votre traitement un jeudi
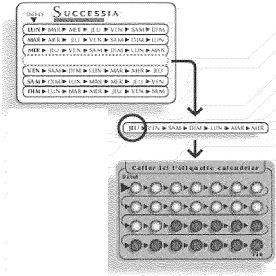
Décoller de son support l'étiquette calendrier commençant le jeudi (bandelette autocollante). Collez cette étiquette calendrier sur l'emplacement réservé situé en haut de votre plaquette.
Prenez votre comprimé chaque jour en suivant strictement le sens des flèches.
Durée du traitement
Selon l'avis de votre médecin.
Symptômes et instructions en cas de surdosage
Si vous avez pris plus de SUCCESSIA 1 mg/0,025 mg, comprimé pelliculé que vous n'auriez du: les signes de surdosage sont habituellement une sensation de douleur au niveau des seins, un gonflement du ventre, des flatulences, des nausées, des vomissements, une irritabilité, des saignements. Aucun traitement spécifique n'est nécessaire.
En cas de persistance des signes, demandez l'avis de votre médecin.
Instructions en cas d'omission d'une ou de plusieurs doses
Si vous oubliez de prendre SUCCESSIA 1 mg/0,025 mg, comprimé pelliculé: si l'oubli d'un comprimé est constaté dans les 24 heures qui suivent l'heure habituelle de la prise, prenez immédiatement le comprimé oublié, puis poursuivez le traitement normalement en prenant le comprimé suivant au moment habituel.
En cas de doute, consultez votre médecin.
Ne prenez pas de dose double pour compenser la dose simple que vous avez oublié de prendre.
Si vous n'avez pas pris de comprimé plusieurs jours de suite, des saignements irréguliers peuvent apparaître.
Effets pouvant apparaître lorsque le traitement par SUCCESSIA 1 mg/0,025 mg, comprimé pelliculé est arrêté: à l'arrêt du traitement, les signes de déficit en estrogènes liés à la ménopause peuvent réapparaître.
4. QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ?
Description des effets indésirables
Comme tous les médicaments, SUCCESSIA 1 mg/0,025 mg, comprimé pelliculé est susceptible d'avoir des effets indésirables, bien que tout le monde n'y soit pas sujet.
Sont fréquemment observés au cours d'un traitement hormonal de la ménopause:
Sont rarement observés:
Si vous remarquez des effets indésirables non mentionnés dans cette notice, ou si certains effets indésirables deviennent graves, veuillez en informer votre médecin ou votre pharmacien.
5. COMMENT CONSERVER SUCCESSIA 1 mg/0,025 mg, comprimé pelliculé ?
Tenir hors de la portée et de la vue des enfants.
Ne pas utiliser SUCCESSIA 1 mg/0,025 mg, comprimé pelliculé après la date de péremption mentionnée sur la boîte.
A conserver dans le conditionnement primaire d'origine.
A conserver à une température ne dépassant pas + 30°C.
Si nécessaire, mises en garde contre certains signes visibles de détérioration
N'utilisez pas SUCCESSIA 1mg/0,025 mg, comprimé pelliculé si vous constatez des signes de détérioration.
Les médicaments ne doivent pas être jetés au tout à l'égout ou avec les ordures ménagères. Demandez à votre pharmacien ce qu'il faut faire des médicaments inutilisés. Ces mesures permettront de protéger l'environnement.
6. INFORMATIONS SUPPLEMENTAIRES
Liste complète des substances actives et des excipients
Que contient SUCCESSIA 1 mg/0,025 mg, comprimé pelliculé ?
Les substances actives sont:
Comprimé beige
Estradiol ....................................................................................................................................... 1,000 mg
Sous forme d'estradiol hémihydraté ................................................................................................. 1,033 mg
Pour un comprimé pelliculé.
Comprimé bleu
Estradiol ....................................................................................................................................... 1,000 mg
Sous forme d'estradiol hémihydraté ................................................................................................. 1,033 mg
Gestodène .................................................................................................................................... 0,025 mg
Pour un comprimé pelliculé.
Les autres composants sont:
Comprimé beige
Lactose monohydraté, amidon de maïs, amidon de maïs modifié, povidone 25000, stéarate de magnésium.
Pelliculage: hypromellose, macrogol 6000, dioxyde de titane, oxyde de fer jaune, oxyde de fer rouge, talc.
Comprimé bleu
Lactose monohydraté, amidon de maïs, amidon de maïs modifié, povidone 25000, stéarate de magnésium.
Pelliculage: hypromellose, macrogol 6000, dioxyde de titane, laque aluminique d'indigotine, talc.
Forme pharmaceutique et contenu
Qu'est-ce que SUCCESSIA 1 mg/0,025 mg, comprimé pelliculé et contenu de l'emballage extérieur ?
SUCCESSIA 1 mg/0,025 mg se présente sous forme de comprimés pelliculés.
Boîtes de 1 plaquette de 28 comprimés (16 comprimés beiges et 12 comprimés bleus).
WYETH PHARMACEUTICALS FRANCE
Coeur Défense - Tour A- La Défense 4
92931 PARIS LA DEFENSE Cedex
WYETH PHARMACEUTICALS FRANCE
Parc d'Activités des Onze Arpents
20, rue Robert Nau
41000 BLOIS
MEDIFA
96/100, avenue de Châteaudun
41000 BLOIS
ou
SODIA
Avenue Robert Schuman
51100 REIMS
Noms du médicament dans les Etats membres de l'Espace Economique Européen
Sans objet.
Date d’approbation de la notice
La dernière date à laquelle cette notice a été approuvée est le {date}.
AMM sous circonstances exceptionnelles
Sans objet.
Des informations détaillées sur ce médicament sont disponibles sur le site Internet de l’Afssaps (France).
Informations réservées aux professionnels de santé
Sans objet.
Sans objet.
